我们的全球检测与审核服务十分全面,助您的产品成功上市
医疗器械具有许多不同用途,从轻伤处理到抢救生命,不一而足。为了确保器械的安全性,目前已建立的一套国际通用的法规条例,各国也有自己一套复杂的规章体系。制造商很难熟知每个国家的特定法规条例,也就很难确认自己的产品是否符合目标市场的要求。
我们是一家高度专业的医疗器械检测和认证机构,提供全面的服务,确保您的产品符合全球市场的要求。服务包括:
国际认证,尤其是针对亚洲、澳大利亚、欧洲、加拿大、俄罗斯、美国以及南美地区的市场要求开展的国际认证。
根据新医疗器械法规(MDR 2017/745)和欧盟体外诊断医疗器械法规(IVDR 2017/746)开展的认证。
在适用标准、条例和法规的要求方面,我们的专家具有丰富经验,可以帮助您成功进军目标市场。 我们的专家、审核人员以及检测实验室遍及全球,随时为您服务。
我们遍布全球的分支机构,为您提供医疗器械的相关服务
德国莱茵TÜV集团在全球范围内拥有独立实验室、专家及审核人员,总有一个在您身边。地图上标出了我们的医疗专家所在地,以及我们的市场准入服务团队能够为您的医疗器械提供服务的扩展地区。
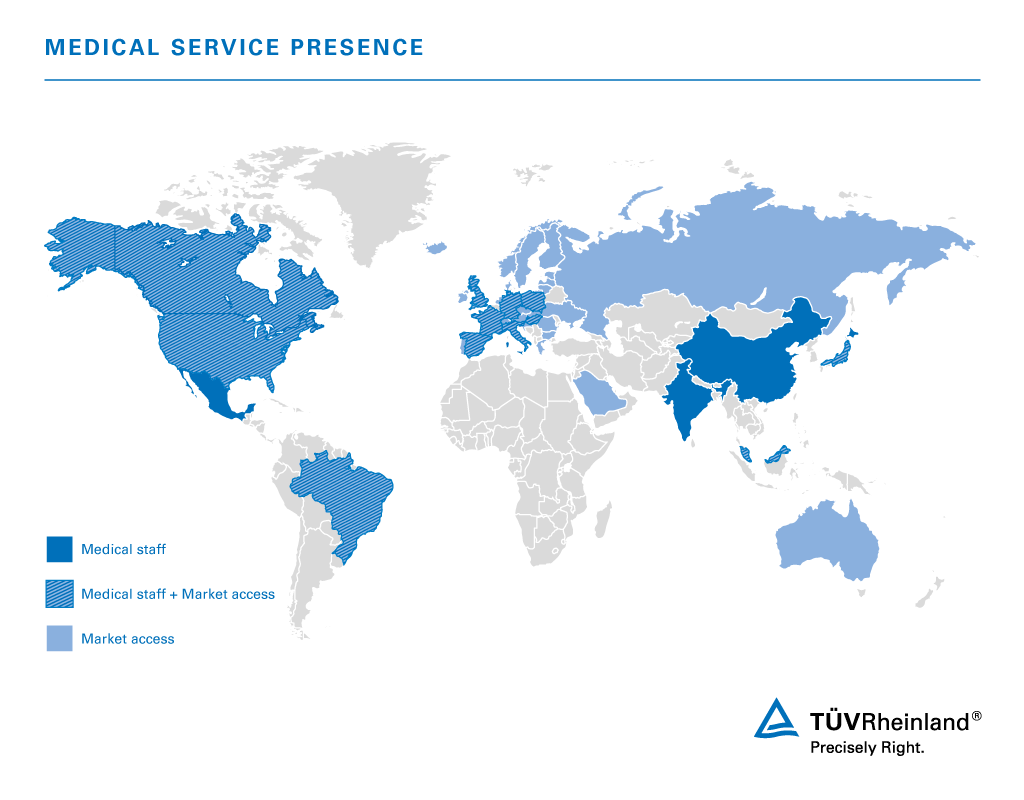
德国莱茵TÜV集团拥有自己的实验室、专家和审核人员,业务遍及全球,为世界各地的客户提供便捷服务。


